È così impossibile recuperare le capacità motorie perdute a seguito di gravi lezioni alla spina dorsale? Recenti studi hanno aperto un importante spiraglio rispetto all’effettiva possibilità di tornare a camminare grazie ad un trapianto di midollo. Le ricerche portate avanti da un’equipe multidisciplinare di ricercatori e professori dell’università di Tel Aviv hanno ottenuto risultati molto promettenti su topi paralizzati.
Nel mondo si studia per rendere l’impossibile possibile
Quante volte si parla di “rompersi la noce del collo” o “spezzarsi la schiena” alludendo ad incidenti irreversibili e con danni permanenti sull’organismo?
Ancora oggi la lesione del midollo spinale è considerata una menomazione a cui non si può porre rimedio alcuno. Questo perché, nonostante i tentativi di ripristino della continuità nervosa e la riabilitazione a cui si sottopongono i pazienti, non è sempre possibile restituire la capacità motoria in caso di gravi lesioni alla spina dorsale.
Fino a questo momento diversi studi hanno visto interessati i ricercatori nel tentativo di ricostruire la spina dorsale. A tal fine sono stati proposti una varietà di approcci che includono il trapianto di diversi tipi di cellule e biomateriali nella zona interessata dalla lesione.
I meccanismi neuronali
Alcuni studi – uno dei quali portato avanti nel 2002 da un gruppo di ricercatori americani – hanno messo in luce la possibilità di impiantare nell’organismo cellule di Schwann. Tali cellule, proprie del sistema nervoso periferico, costituiscono il rivestimento mielinico dell’assone di un neurone. La loro capacità è quella di consentire una velocizzazione nella trasmissione del segnale dai dendriti, siti neuronali che ricevono i segnali esterni, ai terminali assonici (i.e., i siti che si occupano della trasmissione del segnale alle cellule dell’organismo che devono essere stimolate) oppure ai dendriti del neurone successivo (Figura 1).

Il nostro organismo è dotato di una notevole quantità di cellule diverse, che si specializzano in funzione del compito che devono portare avanti nel corso della loro esistenza. Suscitano particolare interesse nella ricerca quelle cellule che ancora non sono specializzate e possono quindi svilupparsi in diverse direzioni, ovvero le cellule staminali. Queste possono essere acquisite da fonti diverse, ad esempio dal cordone ombelicale o da cellule embrionali ai primi stadi dello sviluppo (che sono tessuti estremamente differenziabili), ma anche da tessuti di soggetti adulti.
A seguito dell’estrazione di tali cellule dall’organismo è possibile sviluppare delle culture di cellule indifferenziate, che possono poi essere differenziate in funzione delle necessità.
E’ possibile distinguere vari tipi di cellule staminali, in base alla loro capacità di differenziarsi. Le cellule totipotenti sono in grado di differenziarsi in tutte le tipologie di cellule presenti nell’organismo adulto. L’unica cellula totipotente individuabile nello sviluppo dell’uomo è lo zigote. Le cellule pluripotenti sono quelle cellule in grado di differenziarsi in uno dei tre foglietti germinali: endoderma (epiteli dello stomaco, del tratto gastrointestinale e dei polmoni), mesoderma (muscoli, tessuti connettivi e scheletrici), o ectoderma (epiteli superficiali e ghiandolari e sistema nervoso). Le cellule multipotenti, anche dette mesenchimali, sono in grado, a partire da un singolo ceppo, di generare diversi tipi cellulari limitati in numero. Le cellule unipotenti invece hanno la capacità di differenziarsi in un unico tipo di cellula.
Le cellule neurali
Come per le cellule di Schwann, si è approfondito anche l’impianto di cellule staminali neurali (NSCs) estratte dal tessuto embrionale (in questo articolo) e di cellule staminali progenitrici neurali (NPCs), estratte dal tessuto adulto (in questo articolo) (Figura 2). Queste cellule staminali nello specifico sono capaci di generare diversi tipi di cellule presenti nel cervello adulto, e possono quindi essere utili anche per ricostruire un tessuto nervoso lesionato. Analogamente, in un altra ricerca, si sono affrontati studi anche utilizzando cellule staminali mesenchimali.

La ricerca rivoluzionaria
Una più recente ricerca portata avanti da un gruppo di ricercatori della Shmunis School of Biomedicine and Cancer Research, pubblicata sulla rivista Advanced Sciences, ha dimostrato possibile avere un totale recupero delle capacità motorie nei topi.
Fine ultimo della ricerca, che ad oggi è ancora ai suoi stadi iniziali, è quello di produrre degli impianti di midollo che siano personalizzati e non provochino reazioni di rigetto nel paziente ricevente.
Per il momento lo studio è focalizzato sui roditori: l’esperimento ha previsto un vero e proprio trapianto di tessuto umano ingegnerizzato, che consiste in un tessuto prodotto artificialmente in laboratorio e composto da strutture 3D di biomateriali o di cellule, nei roditori.
Esperimenti analoghi sono stati effettuati sia su roditori con paralisi in fase acuta che in fase cronica. Si parla di paralisi in fase acuta quando l’evento che ha provocato il danneggiamento alla colonna vertebrale (SCI – Spinal Cord Injury) è avvenuto da meno di un anno (tempo considerato rispetto alla vita di un essere umano), in caso di un trauma più lontano nel tempo si parla di paralisi in fase cronica.
Studi attuali per evitare il rigetto
Quando si parla di trapianti (sia di organi che di cellule staminali, come nel caso trattato) il principale problema che si può riscontrare è il rigetto del sistema estraneo al paziente. In queste circostanze l’organo o le cellule staminali impiantate vengono attaccate dallo stesso sistema immunitario del paziente, che tende a distruggerle – causando danni non trascurabili al soggetto.
Per la rigenerazione della spina dorsale lesionata la strategia più comunemente adottata (descritta nello studio qui riportato) consiste nel trapianto di diverse linee cellulari derivate da cellule staminali pluripotenti indotte (iPSCs), ottenute da cellule somatiche del paziente, prima riprogrammate per diventare pluripotenti e dopo differenziate in funzione della tipologia di cellule necessarie per l’impianto che si doveva effettuare.
Si evita, in questo modo, la diretta applicazione sul sito della lesione di cellule indifferenziate. Così facendo si permette alle cellule trapiantate di differenziarsi autonomamente e di interagire con i neuroni dell’ospite in modo da formare assoni che si estendano su lunghe distanze della materia bianca della spina dorsale danneggiata.
In uno studio analizzato dagli stessi ricercatori di Tel Aviv, le cellule trapiantate sono state differenziate già in vivo in tre generazioni neurali senza formare teratomi (i.e., tumori originati da cellule germinali appartenenti a tessuti embrionali e, che si possono sviluppare a partire da cellule staminali pluripotenti). Tali cellule hanno partecipato, a valle dell’intervento, nella rimielinizzazione e nel miglioramento della locomozione del soggetto.
Il problema di questo tipo di impianto risiede nel fatto che le cellule trapiantate impiegano le loro energie per allacciarsi alla sezione di spina dorsale sana. Poiché il tessuto cicatriziale,che si forma nel luogo della lesione – come conseguenza naturale della patofisiologia – non è adatto alla creazione di nuovi tessuti, si potrebbe verificare una massiccia morte cellulare.
Si è pensato quindi di impiantare il tessuto ingegnerizzato non sul tessuto cicatriziale, ma direttamente nel sito della lesione, però i risultati anche in questo caso non sarebbero certi né prevedibili (Figura 3).
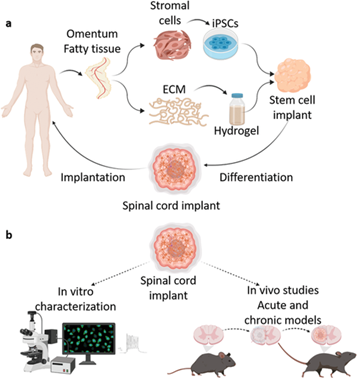
La soluzione
I ricercatori di Tel Aviv, a seguito di studi paralleli a quelli citati, sono riusciti recentemente a sviluppare impianti di tessuti umani derivati da cellule staminali pluripotenti che riescono a fondere perfettamente il profilo immunologico e cellulare del paziente, evitando quindi il rigetto a valle dell’intervento.
Il metodo adottato consiste nel prelievo di una piccola massa di grasso addominale dal paziente. Come tutti i tessuti dell’organismo, anche in questo caso si può distinguere la matrice extracellulare dalle cellule stesse. Sono quindi state estratte dal tessuto le cellule e sono state modificate, così da riportarle alla forma di cellule staminali embrionali – in grado di essere riportate a qualsiasi tipologia di cellula dell’organismo.
La matrice extracellulare, composta principalmente da zuccheri e collagene, ottenuta a seguito dell’estrazione delle cellule dal tessuto, è stata utilizzata per produrre un idrogelo perfettamente compatibile con il paziente, che non provochi una risposta immunitaria nel soggetto. Successivamente, le cellule staminali sono state incapsulate nell’idrogelo ottenuto.
Attraverso un processo simile allo sviluppo embrionale del midollo spinale, le cellule sono state trasformate in tessuto ingegnerizzato strutturato in impianti tridimensionali di reti neurali contenenti motoneuroni.
Gli impianti così ottenuti potrebbero essere introdotti nel sito della lesione in modo da restituire le capacità locomotorie al paziente.
I risultati a seguito dell’applicazione di questi impianti sono stati promettenti.
I roditori affetti da paralisi cronica sono guariti con un’incidenza dell’80%, mentre quelli affetti da paralisi acuta sono guariti con un’incidenza del 100%.
Sviluppi futuri
I ricercatori sono fiduciosi che la tecnologia sviluppata possa essere utile nel trattamento di pazienti umani affetti da paralisi. Questa tecnica, infatti, a partire da una piccola biopsia del paziente e un idrogelo personalizzato, consentirebbe di produrre delle iPSCs specifiche per il singolo paziente, a partire dalle quali generare degli impianti di tessuto ingegnerizzato.
La possibilità di produrre degli impianti che possano rimpiazzare il tessuto cicatrizzato e riescano a recuperare le capacità motorie di una spina dorsale danneggiata nelle persone potrebbe rappresentare un nuovo approccio nella terapia cellulare personalizzata.
Fonti e approfondimenti
- Advanced Science – Regenerating the Injured Spinal Cord at the Chronic Phase by Engineered iPSCs-Derived 3D Neuronal Networks
- PNAS – Multifunctionalized hydrogels foster hNSC maturation in 3D cultures and neural regeneration in spinal cord injuries
- Nature Medicine – Restorative Effects of Human Neural Stem Cell Grafts to the Primate Spinal Cord








